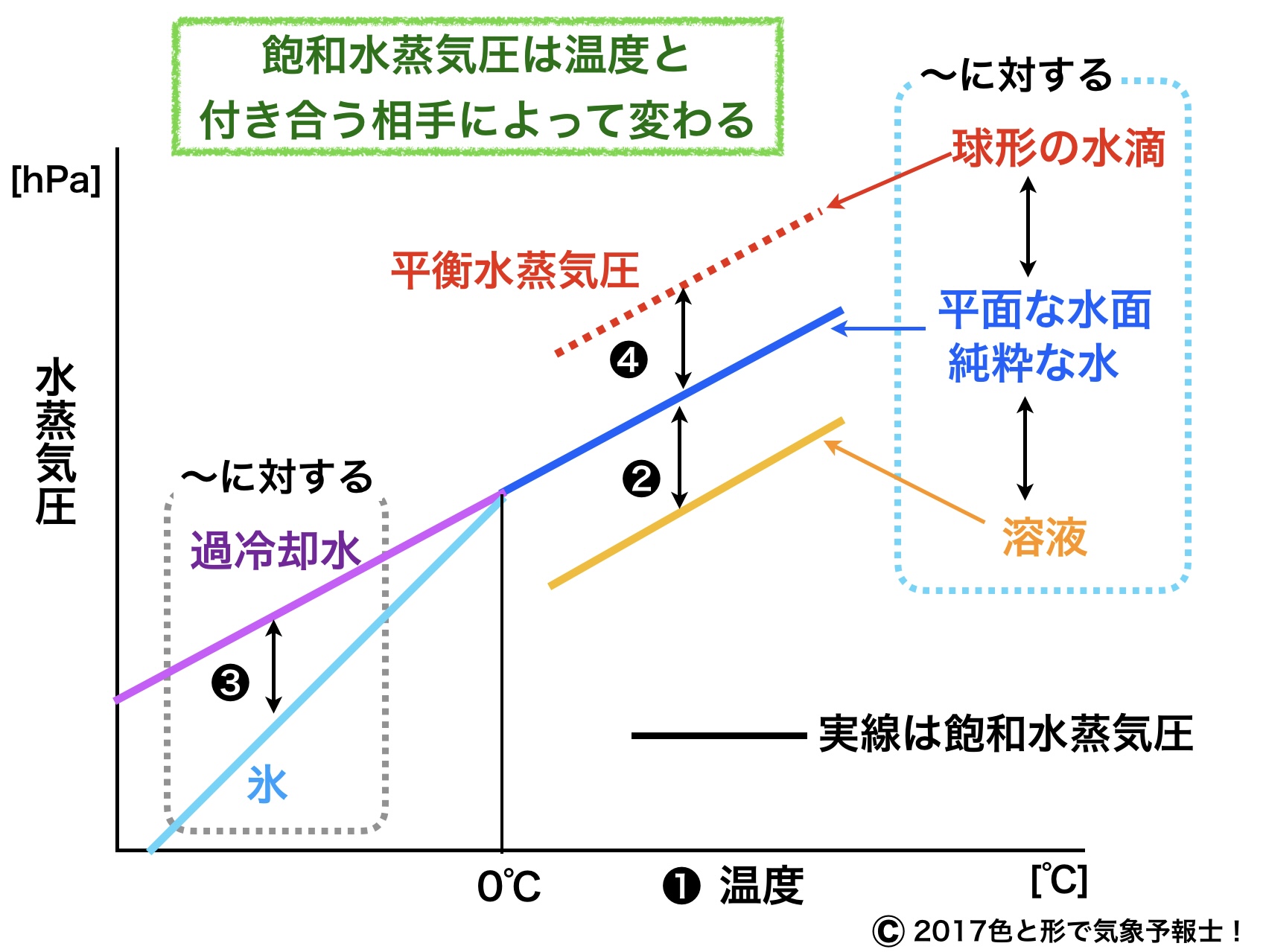
少し前の記事「エーロゾルの役割を水蒸気圧から見る(水滴の生成2)」で、飽和水蒸気圧は相手を選ぶと学びました。言ってみれば付き合う相手によって変わるということです。飽和水蒸気密度についても同様です。
この記事では新たなグラフや模式図を使って、温度による飽和水蒸気圧の変化と付き合う相手による飽和水蒸気圧の変化、2つをまとめて考えていきます。
さらに、相手が2人いる場合どうなるかも調べていきます(何のこと?)
1.温度と飽和水蒸気圧の関係
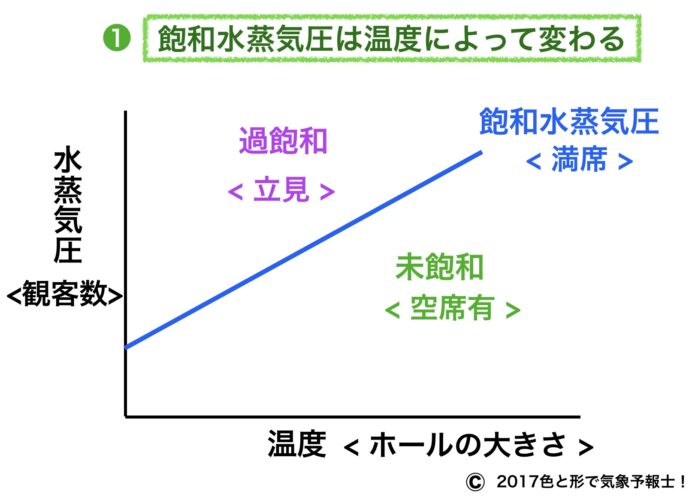
何度か取り上げていますが、今回、温度と飽和水蒸気圧の関係をホールの席に例えて説明します。
温度をホールの大きさに例えると、ホールが大きいほど席を多く置けます。
そこに、水蒸気を示す観客が入ってきます。
観客が席に着き始め、やがて満席になります。この時の観客数が飽和水蒸気圧というわけです。
ホールが大きいほど席が多いのでたくさんの人が席に座れます。つまり飽和水蒸気圧が高いということです。
グラフの飽和水蒸気圧の線の下側は空席がある状態、つまり未飽和です。
線の上側は席に座りきれずに立ち見の人がいる状態、つまり過飽和です。
温度と飽和水蒸気圧の関係はこのようにイメージできるでしょう。
断熱冷却で考えると観客数は変わらないのにホールが勝手に小さくなっていくわけなので、ちょっと怖いですね。
2.純粋な水と溶液
テキストなどに出てくる温度と飽和水蒸気圧の表やグラフは、水分子以外 何も混ざっていない純粋な水(純水)を前提としています。
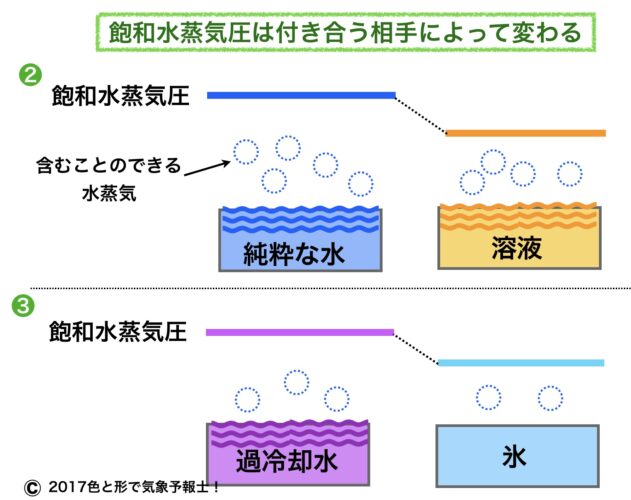
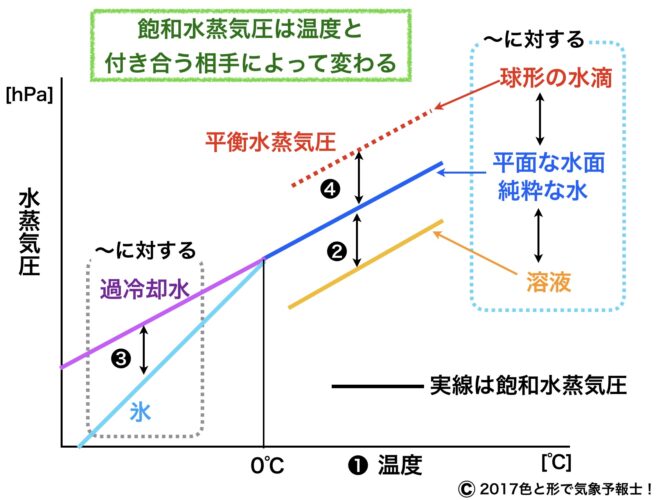
では水が化学物質などが混じった溶液である場合の飽和水蒸気圧はどうでしょうか?模式図の上段❷をご覧ください。
図では含むことのできる水蒸気の量を点線の丸の数~個で表しています。
純水の上の空気が5個の水蒸気を含めるのに対し、溶液の上の空気は4個の水蒸気しか含むことができません。
つまり溶液に対する方が飽和水蒸気圧が低いというわけです。
この点は前述の記事の中でエーロゾルに絡めて扱いました。
3.過冷却水と氷
水は摂氏0℃で氷になります。でも実際には0℃以下でも水のままでいることがあり、これを過冷却水といいます。
上の模式図の下段❸をご覧ください。
過冷却水の上の空気は3個の水蒸気を含むことができます。
対して氷の上の空気が含むことができる水蒸気は2個です。
つまり氷に対しての方が飽和水蒸気圧が低いということです。
4.水滴の半径と平衡水蒸気圧
この話題は前述の「エーロゾルの役割を水蒸気圧から見る(水滴の生成2)」で詳しく取り上げているので、ぜひ読んでみてください。
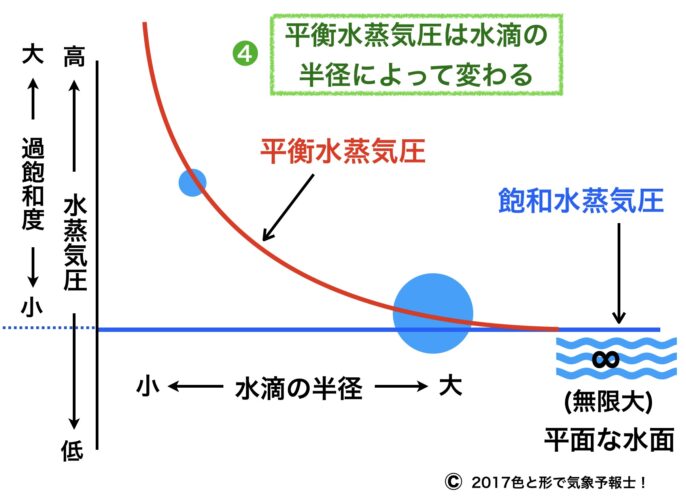
平衡水蒸気圧とは(私の理解では)水滴と周りの水蒸気との間で気液平衡の状態にあるときの水蒸気圧のことです。
つまり水滴から飛び出して来た水蒸気と水滴に飛び込む水蒸気の量が同じであるときの水蒸気圧で飽和水蒸気圧と同じような仕組みになっています。
平衡水蒸気圧は水滴の半径が小さいほど大きく、半径が大きいほど小さくなります。
半径が無限大に大きくなると、それは平面な水面になり平衡水蒸気圧は飽和水蒸気圧と同じになります。
ここまでの説明を一つの模式図で示すとこのようになります。
5.異なる飽和水蒸気圧の対象となる液体が隣接しているとどうなるか?
下の模式図の左上をご覧ください。
2つの容器の片方に純水、もう片方に溶液を入れて隣り合うように置きます。
ここで水蒸気の量を青い丸、まだ含むことができる水蒸気の量を青い点線の丸、限界を超えて存在する水蒸気の量を紫の丸、として表します。
点線の丸があれば未飽和、紫の丸があれば過飽和ということです。
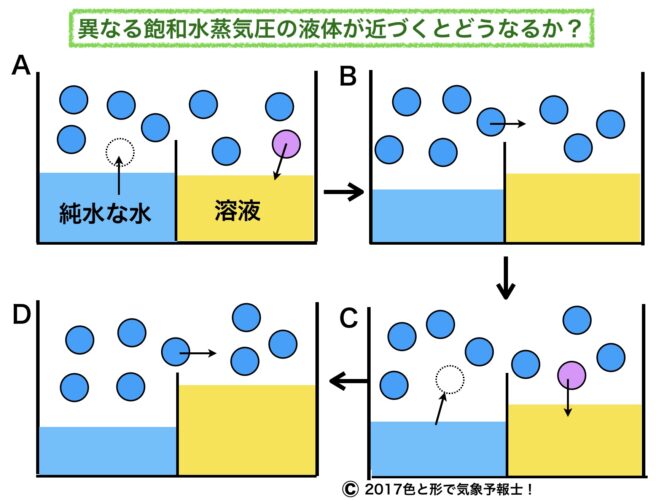
<A>
最初、2つの液体の上に4つずつの丸があります。
純水に対する飽和水蒸気圧を丸5個、溶液に対する飽和水蒸気圧を丸3個とします。
純水の上には水蒸気が4個ありますが、もう1個 水蒸気を含むことができるので、純水から水蒸気が1個飛び出して来ます。
一方、溶液の上にも4個の水蒸気がありますが、溶液に対する飽和水蒸気圧は3個なので1個は過飽和となり溶液に飛び込んでしまいます。
<B>
純水の量は飛び出した水蒸気の分だけ減り、溶液の量は飛び込んだ水蒸気の分だけが増えます。
空気中では純水の上の水蒸気が5個となり、溶液の上の水蒸気は3個になります。
純水の上より溶液の上の方が水蒸気が少なく広々してるので、そちらに1個移動していきます。
<C>
するとまた、純水の上には1個分の空スペースができて水蒸気が1個出て行き、溶液の上では1個余分にあるので、1個溶液に飛び込んでいきます。
<D>
純水の量はさらに減り溶液の量は増えます。
再び、純水の上から溶液の上へと水蒸気1個が移動していきます。
こうしたサイクルを繰り返して純水は減っていき、溶液は増えていきます。
今は純水と溶液を比べて説明しましたが、同じ原理は過冷却水と氷との間でも同様です。
6.まとめ
飽和水蒸気圧は
▶ 温度が低いほど低い
▶ 純粋な水より溶液に対する方が低い
▶ 過冷却水より氷に対する方が低い
平衡水蒸気圧は
▶ 水滴の半径が大きいほど低い
以上の飽和水蒸気圧に関して学んできた内容は、降水粒子の成長に大きく関わってきます。そのプロセスは別の記事で取り上げる予定です。